~従来方法に比べて抗体発現量が約2倍向上~ 抗体医薬品の安定供給を実現するHspa5プロモーターを用いた新たな抗体発現系を開発
2022.05.24
京都産業大学生命科学部 潮田亮准教授らの研究グループは、チャイニーズハムスター卵巣細胞から抗体を発現させる際に、Hspa5プロモーターを用いることで従来の高発現プロモーターに比べて抗体生産性を約2倍向上できることを解明しました。今後、安定した抗体産生が実現できるだけでなく、癌や新型コロナウイルス(COVID-19)などの疾患に対する創薬研究にも寄与できることが期待されます。
リリース日:2022-5-24
本件のポイント
- CHO細胞*1を用いた抗体発現において、トランスクリプトーム解析*2から発現量の高い遺伝子「hspa5*3」を特定した。
- hspa5遺伝子のプロモーター*4「Hspa5p」を用いた抗体産生では、プロテオスタシス*5を維持し、従来の高発現プロモーターに比べて抗体生産性が約2倍向上することが分かった。
- 今回開発した発現系を用いることで、安定した抗体高生産を実現し、抗体医薬品*6の安定供給に貢献するとともに、癌や新型コロナウイルス(COVID-19)など多くの疾患に対する創薬研究に寄与する。
概要
京都産業大学生命科学部の種村裕幸客員研究員、潮田亮准教授らの研究グループは、CHO細胞を用いた抗体発現において、発現量の高い遺伝子「hspa5」を特定し、hspa5遺伝子のプロモーター「Hspa5p」を用いることで、CHO細胞の培養の後半でも抗体の生産量が維持されることを見出しました。本研究成果は、抗体医薬品の安定した製造の実現に貢献できると期待されており、英国ネイチャー・パブリッシング・グループの科学雑誌Scientific Reportsオンライン版(2022年5月24日付)に掲載されました。
背景
近年、免疫グロブリンG (Immunoglobulin G、IgG)などのモノクローナル抗体は、高い特異性と有効性を併せ持つ有望なバイオ医薬品として注目を集めています。1986年にMuromonab-CD3が承認されて以来、モノクローナル抗体を用いた120品目以上の抗体医薬品が上市されています。抗体医薬品の製造には大量の抗体を生産できるCHO細胞が広く用いられています。
本研究では安定した抗体生産の実現に向けて、抗体遺伝子の転写に関わるプロモーターに注目しました。これまで、CHO細胞を用いた抗体発現にはCMVやhEF1αといったプロモーターが使用されてきました。しかし、これらのプロモーターの発現量は、フェドバッチ培養 *7の後半において減少するという問題があります。そこで本研究では、高発現かつ培養後半まで抗体遺伝子の転写量を維持できるプロモーターの取得を目的に、網羅的な遺伝子転写量解析(トランスクリプトーム解析)により新規高発現プロモーターの取得を試みました。
本研究では安定した抗体生産の実現に向けて、抗体遺伝子の転写に関わるプロモーターに注目しました。これまで、CHO細胞を用いた抗体発現にはCMVやhEF1αといったプロモーターが使用されてきました。しかし、これらのプロモーターの発現量は、フェドバッチ培養 *7の後半において減少するという問題があります。そこで本研究では、高発現かつ培養後半まで抗体遺伝子の転写量を維持できるプロモーターの取得を目的に、網羅的な遺伝子転写量解析(トランスクリプトーム解析)により新規高発現プロモーターの取得を試みました。
研究成果
CHO細胞における遺伝子転写量は、使用するクローンや培養条件によって変化する可能性があります。そこで、実製造で高い抗体生産性が得られるプロモーターを取得するため、製造で使用されることが想定される複数のクローン及び培地条件で培養したCHO-K1細胞について培養経時的に細胞サンプルを取得し、トランスクリプトーム解析を実施しました。トランスクリプトーム解析で発現量上位だった遺伝子(図1)のプロモーターを候補として、ルシフェラーゼアッセイ及び抗体発現量評価を実施した結果、トランスクリプトーム解析で培養後半に発現量が向上していたhspa5遺伝子のプロモーター(Hspa5p)を抗体発現に用いることで、コントロールプロモーター(hEF1αp)に対して、培養14日目で1.4倍程度に生産性が向上することを見出しました。
続いて、遺伝子配列解析からプロモーター領域を特定し、プロモーター長を約3.0 kbから約0.6 kbに最適化することにより抗体発現量をさらに向上することに成功しました。Hspa5p下流で各種IgGサブクラスを発現させた結果、いずれもフェドバッチ培養後半まで生産性が維持され、コントロールプロモーター(hEF1αp)と比較して生産性が2倍程度に向上したことから、抗体医薬品製造のための高発現プロモーターとして汎用的に活用できることが確認されました(図2)。
Hspa5は小胞体ストレス *8に応答性のある分子シャペロン *9であるため、小胞体ストレス関連遺伝子発現量を解析しました。その結果、Hspa5p活性すなわち小胞体ストレス応答と、抗体生産量及び重合体含量との間に相関があることが示唆されました。これらの結果から、抗体生産によって生じた小胞体ストレスによる正のフィードバック制御によって、小胞体ストレス関連因子とHspa5pによる抗体生産量が向上するモデルが考えられました(図3)。
続いて、遺伝子配列解析からプロモーター領域を特定し、プロモーター長を約3.0 kbから約0.6 kbに最適化することにより抗体発現量をさらに向上することに成功しました。Hspa5p下流で各種IgGサブクラスを発現させた結果、いずれもフェドバッチ培養後半まで生産性が維持され、コントロールプロモーター(hEF1αp)と比較して生産性が2倍程度に向上したことから、抗体医薬品製造のための高発現プロモーターとして汎用的に活用できることが確認されました(図2)。
Hspa5は小胞体ストレス *8に応答性のある分子シャペロン *9であるため、小胞体ストレス関連遺伝子発現量を解析しました。その結果、Hspa5p活性すなわち小胞体ストレス応答と、抗体生産量及び重合体含量との間に相関があることが示唆されました。これらの結果から、抗体生産によって生じた小胞体ストレスによる正のフィードバック制御によって、小胞体ストレス関連因子とHspa5pによる抗体生産量が向上するモデルが考えられました(図3)。
今後の展開
今回、トランスクリプトーム解析の結果から、フェドバッチ培養後半まで抗体生産が安定して高く維持されるプロモーターとして、Hspa5pを見出しました。さらに、Hspa5pによる抗体生産が小胞体ストレス応答と関連する可能性のあるデータも取得しました。小胞体ストレス応答によってどのようにHspa5pによる抗体生産性が向上しているか、現時点ではその詳細なメカニズムは不明な点が多いです。
タンパク質の品質管理機構に関わる小胞体ストレス応答関連遺伝子の発現量と抗体質生産量が連動して向上する可能性を得ました。Hspa5pを利用することで小胞体でのタンパク質環境の恒常性(プロテオスタシス)を維持し、安定した抗体産生が実現できると期待しています。また、Hspa5pは癌などの多くの疾患に関与しており、近年では新型コロナウイルス(COVID-19)感染にも関与していることが報告されています。よって、Hspa5pの発現制御メカニズムを解明することは安定したタンパク質生産の実現のみならず、それらの疾患に対する創薬研究にも寄与できると考えています。
タンパク質の品質管理機構に関わる小胞体ストレス応答関連遺伝子の発現量と抗体質生産量が連動して向上する可能性を得ました。Hspa5pを利用することで小胞体でのタンパク質環境の恒常性(プロテオスタシス)を維持し、安定した抗体産生が実現できると期待しています。また、Hspa5pは癌などの多くの疾患に関与しており、近年では新型コロナウイルス(COVID-19)感染にも関与していることが報告されています。よって、Hspa5pの発現制御メカニズムを解明することは安定したタンパク質生産の実現のみならず、それらの疾患に対する創薬研究にも寄与できると考えています。
謝辞
本研究は、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)「プロテオスタシスの理解と革新的医療の創出」研究開発領域(研究開発総括:永田和宏)における研究開発課題「プロテオスタシスにおけるタンパク質構造形成機構の包括的解明」(研究開発代表者:田口英樹)の支援を受けて行われました。
また、本研究の一部は、経済産業省の「平成25年度個別化医療に向けた次世代医薬品創出基盤技術開発(国際基準に適合した次世代抗体医薬等製造技術)」及び平成26年度次世代医療・診断実現のための創薬基盤技術開発事業(国際基準に適合した次世代抗体医薬等製造技術))」、及び国立研究開発法人日本医療研究開発機構(AMED)の「次世代医療・診断実現のための創薬基盤技術開発事業(JP17ae0101003)」の支援によって行われました。
また、本研究の一部は、経済産業省の「平成25年度個別化医療に向けた次世代医薬品創出基盤技術開発(国際基準に適合した次世代抗体医薬等製造技術)」及び平成26年度次世代医療・診断実現のための創薬基盤技術開発事業(国際基準に適合した次世代抗体医薬等製造技術))」、及び国立研究開発法人日本医療研究開発機構(AMED)の「次世代医療・診断実現のための創薬基盤技術開発事業(JP17ae0101003)」の支援によって行われました。
用語・事項の解説
*1 CHO細胞
チャイニーズハムスターの卵巣から取得された細胞。遺伝子導入によりタンパク質を分泌する細胞として広く使用されている。CHO-K1、CHO-DG44、およびCHO-Sなどの様々な系統が樹立され、数多くのバイオ医薬品の製造に用いられている。
*2 トランスクリプトーム解析
次世代シーケンサーを用いて取得したRNA配列データから、細胞内の各遺伝子の発現量を網羅的に解析する手法。
*3 hspa5
Hspa5をコードする遺伝子。Hspa5はHeat shock protein 70ファミリーに属する小胞体内分子シャペロン。別名は、BiP、GRP78。小胞体ストレスによって発現が誘導される。小胞体でのタンパク質の折り畳みに関わることでタンパク質品質管理に関与する。
*4 プロモーター
遺伝子の上流に位置するDNA配列であり、遺伝子からmRNAが転写される量を調整する。
*5 プロテオスタシス
タンパク質環境の恒常性。細胞が健康に生育するためには、タンパク質の発現・局在制御、分子シャペロンによる折り畳み、タンパク質分解などによりタンパク質品質管理が正常に働き、その恒常性が常に維持される必要がある。
*6 抗体医薬品
抗体は生体分子と特異的に結合する化合物である。構造によってサブクラスに大別され、抗体医薬品としては主にIgG1、IgG2、IgG4Proが用いられる。
*7 フェドバッチ培養
CHO細胞の培養法の一つ。培養槽内に細胞を播種した後、細胞増殖に応じて新鮮培地を添加していき、培地成分の消費によって減少した成分を補う。培養開始後に一定の細胞密度までは細胞が増殖するが、代謝老廃物の蓄積などにともない増殖が停止し、以降細胞生存率が低下する。
*8 小胞体ストレス
小胞体は細胞内に存在する細胞小器官の1つであり、タンパク質合成、Ca2+の貯蔵や脂質合成の場など様々な役割を持つ。小胞体ストレスは、小胞体に構造異常タンパク質や正常な修飾を受けていないタンパク質が蓄積することで小胞体にストレスがかかった状態をさす。小胞体ストレス応答とは、ストレスの予防、ストレスからの回復などを担う細胞システムのことである。
*9 分子シャペロン
他のタンパク質の正しいフォールディング(折り畳み)を助けるタンパク質の総称。
論文情報
| タイトル | 「Development of a stable antibody production system utilizing an Hspa5 promoter in CHO cells」 (Hspa5プロモーターを用いたCHO細胞における抗体安定発現系の構築) |
|---|---|
| 掲載誌 | 英国科学雑誌「Scientific reports」(オンライン版) |
| 掲載日 | 2022年5月24日 18:00 (日本時間) |
| 著者 | 種村 裕幸1ac 、増田 兼治c 、奥村 武c 、都木 栄里c 、梶原 大介c 、柿原 博文c 、野中 浩一c 、 潮田 亮2ab (1筆頭著者、2責任著者) (所属 : a京都産業大学生命科学部、 b京都産業大学タンパク質動態研究所、c第一三共株式会社) |
| DOI | 10.1038/s41598-022-11342-1 |
参考図
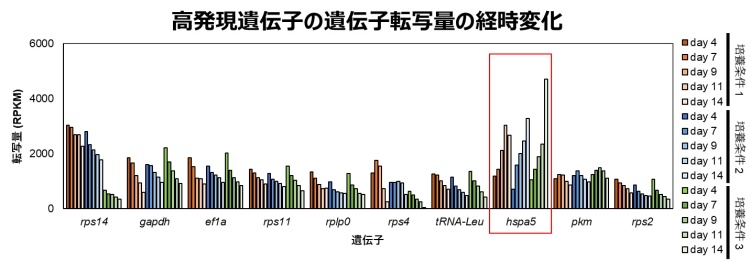
抗体の発現量の高い遺伝子のほとんどが培養後半に発現量が低下するのに対し、hspa5遺伝子が培養後半に発現量が向上することがトランスクリプトーム解析によって示された。
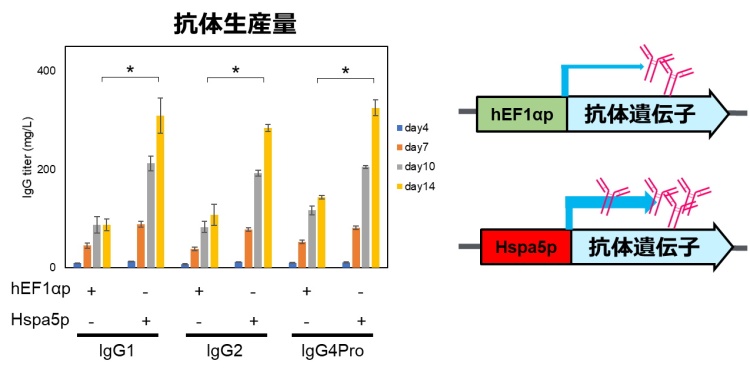
プロモーター長を最適化したHspa5プロモーターを抗体発現に用いることで、コントロールプロモーター(hEF1αp)と比較して各種抗体サブクラスの培養14日目の抗体生産が2倍程度に向上した。
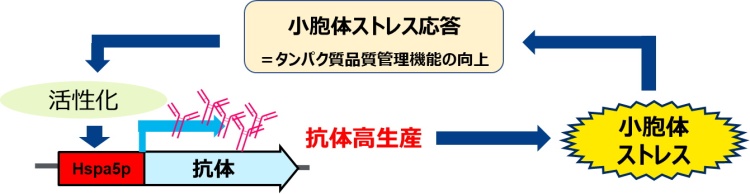
Hspa5プロモーターを抗体発現に用いることで、抗体生産によって生じた小胞体ストレスによる正のフィードバック制御によって、小胞体ストレス関連因子とHspa5pによる抗体生産量が向上することが示唆された。
- お問い合わせ先
-
内容について:京都産業大学生命科学部 潮田 亮 准教授
〒603‐8555 京都市北区上賀茂本山
E-Mail: ryo3ussy3@cc.kyoto-su.ac.jp
取材について:京都産業大学 広報部
Tel.075-705-1411
