タンパク質動態研究所の永田 和宏 所長らが 小胞体ストレス応答伝達タンパク質IRE1αの新規調節因子として 小胞体分子シャペロンHsp47を同定
2018.01.19
京都産業大学タンパク質動態研究所の永田 和宏 所長(京都産業大学 総合生命科学部教授)、伊藤 進也研究員と海外研究者からなる研究グループは、小胞体ストレス応答における重要なシグナル伝達タンパク質であるIRE1αの新規調節因子として、小胞体分子シャペロンHsp47を同定しました。
本研究成果は、1月18日付の米国学術誌「Molecular Cell(オンライン版)」に掲載され、表紙にも採用されました。
リリース日:2018-01-19
論文タイトル
Interactome screening identifies the ER luminal chaperone Hsp47 as a novel regulator of the unfolded protein response (UPR) transducer IRE1α
(和訳:相互作用スクリーニングによりUPRセンサーIRE1αの新規調節因子として小胞体分子シャペロンHsp47が同定された)。
(和訳:相互作用スクリーニングによりUPRセンサーIRE1αの新規調節因子として小胞体分子シャペロンHsp47が同定された)。
著者
Denisse Sepulveda*, Diego Rojas-Rivera*, Diego A. Rodríguez*, Jody Groenendyk, Andres Köhler, Cynthia Lebeaupin, Shinya Ito, Hery Urra, Amado Carreras-Sureda, Younis Hazari, Mireille Vasseur-Cognet, Maruf MU Ali, Eric Chevet, Gisela Campos, Patricio Godoy, Tomas Vaisar, Béatrice Bailly-Maitre, Kazuhiro Nagata, Marek Michalak, Jimena Sierralta and Claudio Hetz#.。
概要
Hsp47は、京都産業大学の永田和宏教授が1986年に発見した、コラーゲン特異的分子シャペロンです。Hsp47が欠損するとコラーゲン合成が阻害され、マウスの発生は障害されます。Hsp47はコラーゲン合成に必須の因子であるだけではなく、コラーゲンが異常に蓄積する病態、たとえば肝硬変、肺線維症を初めとする、種々の線維化疾患においてはコラーゲン合成を過剰に促進して、線維化を増悪させる因子であることも、永田研究室のこれまでの研究から明らかになっており、Hsp47は線維化疾患治療薬のターゲットとして、世界の多くの研究室、製薬企業において研究が進められています。今回、Hsp47が従来知られていたコラーゲン合成とはまったく異なった機能を持っていることが明らかにされました。
背景
インスリンなど分泌タンパク質が作られる場所である小胞体では、小胞体ストレス応答(Unfold Protein Response ; UPRER)と呼ばれる動的なシグナル伝達ネットワークによってタンパク質の恒常性が制御されています。 UPRERは京都大学 森 和俊先生やUCSFのPeter Walter博士の研究がノーベル賞候補になるなど、大きな注目を集めている分野です。
小胞体膜タンパク質であるIRE1αは、主要なUPR伝達因子として働き、小胞体がストレスを受けたときの細胞運命を左右する重要なRNA切断酵素です。小胞体ストレス時に分子シャペロンBipが IRE1αから離れ、IRE1αは多量体になることで活性化し、転写因子XBP1をコードするmRNAのスプライシングを触媒します。スプライシングされたXBP1 mRNAから転写因子XBP1sが翻訳され、小胞体関連分解を行うタンパク質や酸化還元酵素の量を増加させます。この反応によって、ストレスを受けた細胞の小胞体内部のタンパク質恒常性を維持し、細胞の生存にとって必須のストレス防御機構となっています。
このように、小胞体ストレス時に様々な応答を出力するIRE1αは、UPRosomeと呼ばれるタンパク質間での動的なIRE1α複合体を形成し、下流のシグナル伝達経路および他のストレス経路とのクロストークを制御しています。
小胞体膜タンパク質であるIRE1αは、主要なUPR伝達因子として働き、小胞体がストレスを受けたときの細胞運命を左右する重要なRNA切断酵素です。小胞体ストレス時に分子シャペロンBipが IRE1αから離れ、IRE1αは多量体になることで活性化し、転写因子XBP1をコードするmRNAのスプライシングを触媒します。スプライシングされたXBP1 mRNAから転写因子XBP1sが翻訳され、小胞体関連分解を行うタンパク質や酸化還元酵素の量を増加させます。この反応によって、ストレスを受けた細胞の小胞体内部のタンパク質恒常性を維持し、細胞の生存にとって必須のストレス防御機構となっています。
このように、小胞体ストレス時に様々な応答を出力するIRE1αは、UPRosomeと呼ばれるタンパク質間での動的なIRE1α複合体を形成し、下流のシグナル伝達経路および他のストレス経路とのクロストークを制御しています。
研究方法・成果
チリ大学のDenisse Sepulveda研究員、Claudio Hetz教授らを中心に、カナダのアルバータ大学のMarek Michalak教授および本学の伊藤進也研究員、永田和宏教授らが加わった研究グループが、IRE1αとの相互作用スクリーニングを行ったところ、IRE1αを介したUPRの新規調節因子として小胞体に局在する分子シャペロンHsp47がヒットしました。 In vitroの実験からは、Hsp47が直接IRE1αの内腔部分に高い親和性で結合すること、Hsp47とIRE1αの相互作用はBipとIRE1αの相互作用と競合し、BipのIRE1αからの解離を促進することでIRE1αの多量体化を促すことが分かりました。
また、細胞を用いた実験でもHsp47がIRE1αとの相互作用を介してIRE1αシグナル伝達を誘発することが示されました(図1参照)。さらに、Hsp47を肝臓特異的に欠損させたマウスを用いた実験おいても、小胞体ストレス時のタンパク質恒常性維持にはHsp47が重要であることが明らかになりました。
これらのことより、小胞体ストレス応答における重要なシグナル伝達タンパク質であるIRE1αの新規調節因子としてHsp47を同定することができました。
また、細胞を用いた実験でもHsp47がIRE1αとの相互作用を介してIRE1αシグナル伝達を誘発することが示されました(図1参照)。さらに、Hsp47を肝臓特異的に欠損させたマウスを用いた実験おいても、小胞体ストレス時のタンパク質恒常性維持にはHsp47が重要であることが明らかになりました。
これらのことより、小胞体ストレス応答における重要なシグナル伝達タンパク質であるIRE1αの新規調節因子としてHsp47を同定することができました。
今後の展開
我々は、Hsp47がIRE1αの活性を調整する分子シャペロンネットワークの一部であり、適切な小胞体ストレス応答の閾値を調整していると考えています。Hsp47は、永田研究室によって、コラーゲンの合成、分泌に必須の分子シャペロンであるとされてきましたが、それが小胞体ストレスへの防御機構の制御にも関与する可能性が生まれ、今後従来知られているのとは別の制御機構の研究が進展する可能性が出てきました。小胞体におけるタンパク質の品質管理機構は、アルツハイマー病をはじめとする神経変性疾患に密接な関係を持っていますので、それら治療法の開発への貢献も期待されます。
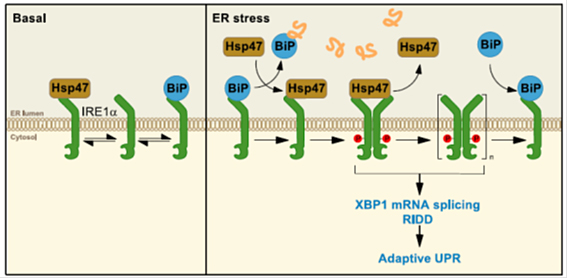
通常時、IRE1αは分子シャペロンBipとの相互作用により不活性型である単量体に維持されています(左図)。小胞体ストレス時、分子シャペロンHsp47がIRE1αに結合し、Bipの解離を誘導することで、IRE1αの活性型である多量体化を促進します。活性化されたIRE1αはUPRシグナルの伝達を適切に行います。小胞体ストレス応答後期でHsp47はIRE1αから離れていき、通常時の状態に戻ります(右図)。
- お問い合わせ先
-
京都産業大学タンパク質動態研究所
永田 和宏 所長研究室Tel:075-705-3090
E-Mail:nagata@cc.kyoto-su.ac.jp
